
藥包材質(zhì)量穩(wěn)定性要求
《藥品質(zhì)量生產(chǎn)管理規(guī)范(2010年修訂)》第一章第三條規(guī)定,“本規(guī)范作為質(zhì)量管理
體系的一部分,是藥品生產(chǎn)管理和質(zhì)量控制的基本要求,旨在……確保持續(xù)穩(wěn)定地生產(chǎn)出符合預(yù)定用途和注冊(cè)要求的藥品。”
第二章第六條規(guī)定,“企業(yè)高層管理人員應(yīng)當(dāng)確保實(shí)現(xiàn)既定的質(zhì)量目標(biāo),不同層次的人員以及供應(yīng)商、經(jīng)銷商應(yīng)當(dāng)共同參與并承擔(dān)各自的責(zé)任。”
其實(shí),藥品質(zhì)量的持續(xù)穩(wěn)定雖然是對(duì)藥品生產(chǎn)質(zhì)量的要求,也是對(duì)直接接觸藥品的包裝材料的生產(chǎn)質(zhì)量的要求。這是因?yàn)樗幤焚|(zhì)量取決于生產(chǎn)工藝、原輔材料、包裝材料、生產(chǎn)設(shè)備、生產(chǎn)環(huán)境等多種因素,其中直接接觸藥品的包裝材料是重要因素之一。而且,在《藥品質(zhì)量生產(chǎn)管理規(guī)范(2010年修訂)》中,關(guān)于直接接觸藥品的包裝材料的管理與控制要求已經(jīng)和原輔材料是一樣的了。
為了實(shí)現(xiàn)這項(xiàng)要求,制藥企業(yè)必定要對(duì)責(zé)任進(jìn)行分解,其中藥包材的質(zhì)量責(zé)任主要由藥包材企業(yè)承擔(dān)。
《藥品質(zhì)量生產(chǎn)管理規(guī)范(2010年修訂)》發(fā)布之日,國(guó)家食品藥品監(jiān)督管理局就下發(fā)通知:自
面對(duì)國(guó)家對(duì)藥品生產(chǎn)企業(yè)提出的諸多要求,藥包材企業(yè)作為藥品生產(chǎn)企業(yè)的主要供應(yīng)商,必須充分認(rèn)識(shí)到藥包材質(zhì)量穩(wěn)定性管理的重要性和迫切性,并及時(shí)采取措施以滿足這項(xiàng)要求。
目前藥包材企業(yè)普遍規(guī)模較小,對(duì)藥包材質(zhì)量管理相關(guān)理論的研究還不完善,僅局限于
滿足國(guó)家食品藥品監(jiān)督管理局第13號(hào)令的審查要求,以此取得注冊(cè)證,然后通過(guò)GB/T19001質(zhì)量體系認(rèn)證,就認(rèn)為達(dá)到了質(zhì)量穩(wěn)定性要求。實(shí)際上,如果不能按照科學(xué)的管理方法對(duì)藥包材質(zhì)量進(jìn)行穩(wěn)定性管理,藥包材質(zhì)量缺陷的發(fā)生頻率就很高,這樣就只能依靠?jī)r(jià)格優(yōu)勢(shì)來(lái)?yè)屨际袌?chǎng),給藥品質(zhì)量的穩(wěn)定性帶來(lái)較大隱患。
控制論分析
ISO/TC176組織發(fā)布了質(zhì)量管理八項(xiàng)原則的第五項(xiàng)為“管理的系統(tǒng)方法”。也就是說(shuō)企業(yè)的質(zhì)量管理工作要作為一個(gè)系統(tǒng)來(lái)管理,這樣才能對(duì)產(chǎn)品質(zhì)量的穩(wěn)定性進(jìn)行有效控制。而要想達(dá)到這個(gè)目的,就必須引進(jìn)控制論。
錢學(xué)森指出:“控制論的對(duì)象是系統(tǒng)”;“為了實(shí)現(xiàn)系統(tǒng)自身的穩(wěn)定和功能,系統(tǒng)需要取得、使用、保持和傳遞能量、材料和信息,也需要對(duì)系統(tǒng)的各個(gè)構(gòu)成部分進(jìn)行組織”;“控制論研究系統(tǒng)各個(gè)部分如何進(jìn)行組織,以便實(shí)現(xiàn)系統(tǒng)的穩(wěn)定和有目的的行為”。
控制論對(duì)系統(tǒng)穩(wěn)定性的控制主要有三種模型:前饋控制、同期控制和反饋控制(如圖1所示)。
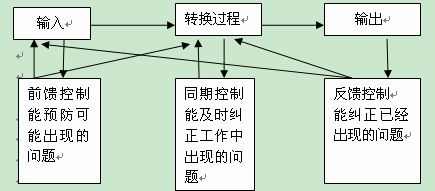
圖1 控制論對(duì)系統(tǒng)穩(wěn)定性的控制模型
前饋控制是指外部條件還沒(méi)有影響到控制對(duì)象之前,就進(jìn)行預(yù)測(cè)、控制。例如,當(dāng)原輔材料供應(yīng)商的預(yù)期發(fā)生改變時(shí),就要對(duì)準(zhǔn)新供應(yīng)商進(jìn)行嚴(yán)格的準(zhǔn)入審查,包括技術(shù)交流、樣品試驗(yàn)、現(xiàn)場(chǎng)考察、質(zhì)量審計(jì)等,經(jīng)過(guò)QA審批以后才可以正式變更。
同期控制是指偏差在剛剛發(fā)生或發(fā)生不久時(shí),就能立即被測(cè)定出來(lái),并迅速查明原因和采取糾正行為。例如,當(dāng)工序檢驗(yàn)人員發(fā)現(xiàn)產(chǎn)品缺陷時(shí),應(yīng)立即通知生產(chǎn)人員加以調(diào)整,將問(wèn)題消滅在萌芽狀態(tài),以避免嚴(yán)重質(zhì)量事故的發(fā)生。
反饋控制是指分析工作的執(zhí)行結(jié)果,然后將結(jié)果與控制標(biāo)準(zhǔn)進(jìn)行比較,當(dāng)發(fā)現(xiàn)已經(jīng)或即將出現(xiàn)的偏差后,分析其產(chǎn)生的原因以及對(duì)未來(lái)的可能影響,及時(shí)擬定糾正措施并予以實(shí)施,以防止偏差的繼續(xù)發(fā)展或再度發(fā)生。例如當(dāng)客戶投訴時(shí),要及時(shí)查明原因并采取措施,以避免問(wèn)題的再度發(fā)生。
因此,藥包材企業(yè)在質(zhì)量管理工作中,只有按照控制論的要求,采取前饋控制、同期控制和反饋控制三種,才能保證藥包材質(zhì)量的穩(wěn)定性,進(jìn)而保證藥品質(zhì)量的穩(wěn)定。
實(shí)施辦法
1、體系文件的建立
藥包材企業(yè)應(yīng)按照GB/T19001質(zhì)量管理體系標(biāo)準(zhǔn),并結(jié)合國(guó)家藥監(jiān)局第13號(hào)令,建立
文件化的質(zhì)量體系。體系文件分為三級(jí),即質(zhì)量手冊(cè)、程序文件、作業(yè)文件和相關(guān)記錄。其中質(zhì)量手冊(cè)是對(duì)質(zhì)量體系作概括表述、闡述及指導(dǎo)質(zhì)量體系實(shí)踐的主要文件,是企業(yè)質(zhì)量管理和質(zhì)量保證活動(dòng)應(yīng)長(zhǎng)期遵循的綱領(lǐng)性文件;程序文件是為進(jìn)行某項(xiàng)活動(dòng)或過(guò)程所規(guī)定的途徑而編寫的文件;作業(yè)文件在GMP的術(shù)語(yǔ)中通常又稱作標(biāo)準(zhǔn)操作程序(SOP),主要是指經(jīng)批準(zhǔn)用來(lái)指導(dǎo)設(shè)備操作、維護(hù)與清潔、驗(yàn)證、環(huán)境控制、取樣和檢驗(yàn)等藥品生產(chǎn)活動(dòng)的通用性文件。
2、變更控制體系的建立
有的藥包材企業(yè)認(rèn)為進(jìn)行到這一步質(zhì)量體系就已經(jīng)建立了,藥品質(zhì)量就有保障了,就可以高枕無(wú)憂了,實(shí)則不然。
質(zhì)量體系在運(yùn)行過(guò)程中,當(dāng)初制定文件所依據(jù)的條件會(huì)發(fā)生變化,因此按照前饋控制的要求,體系文件也必須隨之進(jìn)行變更,而且對(duì)變更必須進(jìn)行控制,這樣才能使質(zhì)量體系文件符合實(shí)際情況,避免“兩張皮”現(xiàn)象。在體系運(yùn)行過(guò)程中,還要隨時(shí)進(jìn)行檢查,發(fā)現(xiàn)問(wèn)題及時(shí)糾正,實(shí)行同期控制。此外,如果體系文件未得到嚴(yán)格執(zhí)行,就會(huì)導(dǎo)致偏差的產(chǎn)生,嚴(yán)重時(shí)甚至?xí)绊懏a(chǎn)品質(zhì)量,所以按照反饋控制的要求,必須對(duì)偏差進(jìn)行控制,這樣才能完全實(shí)現(xiàn)對(duì)產(chǎn)品質(zhì)量的的穩(wěn)定性管理。
因此,按照前饋控制模型,藥包材企業(yè)還必須在質(zhì)量體系當(dāng)中建立變更控制系統(tǒng),對(duì)所有影響產(chǎn)品質(zhì)量的變更進(jìn)行評(píng)估和管理。
3、變更控制流程
所有針對(duì)原輔料、包裝材料、質(zhì)量標(biāo)準(zhǔn)、檢驗(yàn)方法、操作規(guī)程、廠房、設(shè)施、設(shè)備、儀器、生產(chǎn)工藝和計(jì)算機(jī)軟件的變更,都必須履行申請(qǐng)、評(píng)估、審核、批準(zhǔn)的程序以后才能實(shí)施。質(zhì)量管理部門應(yīng)當(dāng)指定專人負(fù)責(zé)變更控制。
(1)評(píng)估
評(píng)估變更對(duì)產(chǎn)品質(zhì)量的潛在影響。企業(yè)可根據(jù)變更的性質(zhì)、范圍、對(duì)產(chǎn)品質(zhì)量潛在影響的程度將變更分類(如主要、次要變更)。判斷變更所需的驗(yàn)證、額外的檢驗(yàn)以及穩(wěn)定性考察應(yīng)當(dāng)有科學(xué)依據(jù)。
(2)審核批準(zhǔn)
與產(chǎn)品質(zhì)量有關(guān)的變更由申請(qǐng)部門提出后,應(yīng)當(dāng)經(jīng)過(guò)評(píng)估、制定實(shí)施計(jì)劃并明確實(shí)施職責(zé),最終由質(zhì)量管理部門審核批準(zhǔn)。有的變更還需要經(jīng)國(guó)家食品藥品監(jiān)督管理局批準(zhǔn)后方可實(shí)施。變更實(shí)施應(yīng)當(dāng)有相應(yīng)的完整記錄,確保在與變更相關(guān)的文件均已修訂以后再實(shí)施變更。質(zhì)量管理部門負(fù)責(zé)保存所有變更的文件和記錄。
(3)監(jiān)控
改變?cè)o料、生產(chǎn)工藝、主要生產(chǎn)設(shè)備以及其他影響產(chǎn)品質(zhì)量的主要因素時(shí),還應(yīng)當(dāng)對(duì)變更實(shí)施后最初的至少三個(gè)批次的產(chǎn)品質(zhì)量進(jìn)行監(jiān)控。
按照同期控制模型,藥包材企業(yè)應(yīng)該要求執(zhí)行人員按規(guī)定的標(biāo)準(zhǔn)化程序完成工作,以保證業(yè)務(wù)處理質(zhì)量達(dá)到控制目標(biāo)和要求。同期控制要求按照控制的原則進(jìn)行程序設(shè)置,所有的主要業(yè)務(wù)活動(dòng)都要建立切實(shí)可行的辦理程序。例如,按照生產(chǎn)流程,每道工序的最終點(diǎn)為程序控制點(diǎn),每道工序的終點(diǎn)的生產(chǎn)者為質(zhì)量控制者,其對(duì)不合格的加工、 不合格的配制有責(zé)任也有權(quán)提出改正,以使每個(gè)人在生產(chǎn)過(guò)程中都受到監(jiān)控。
同期控制可避免業(yè)務(wù)工作的無(wú)章可循、職責(zé)不清、相互推諉,有利于及時(shí)處理業(yè)務(wù)、提高工作效率,以及追究有關(guān)責(zé)任人的責(zé)任。
(4)偏差管理
按照反饋控制模型,藥包材企業(yè)還必須在質(zhì)量體系當(dāng)中建立偏差處理系統(tǒng),對(duì)所有影響產(chǎn)品質(zhì)量的偏差進(jìn)行評(píng)估和管理。
企業(yè)各部門負(fù)責(zé)人應(yīng)當(dāng)確保所有人員正確執(zhí)行生產(chǎn)工藝、質(zhì)量標(biāo)準(zhǔn)、檢驗(yàn)方法和操作規(guī)程,防止偏差的產(chǎn)生。事實(shí)上,偏差的產(chǎn)生是不可避免的,因此應(yīng)當(dāng)建立偏差處理的操作規(guī)程,規(guī)定偏差的報(bào)告、記錄、調(diào)查、處理以及所采取的糾正措施,并進(jìn)行相應(yīng)記錄,使偏差降至最小。
對(duì)任何偏差都應(yīng)當(dāng)評(píng)估其對(duì)產(chǎn)品質(zhì)量的潛在影響。企業(yè)可以根據(jù)偏差的性質(zhì)、范圍、對(duì)產(chǎn)品質(zhì)量潛在影響的程度將偏差分類(如重大、次要偏差),對(duì)重大偏差的評(píng)估還應(yīng)當(dāng)考慮是否需要對(duì)產(chǎn)品進(jìn)行額外的檢驗(yàn)以及對(duì)產(chǎn)品有效期的影響,必要時(shí),應(yīng)當(dāng)對(duì)涉及重大偏差的產(chǎn)品生產(chǎn)進(jìn)行穩(wěn)定性考察。
任何偏離生產(chǎn)工藝、質(zhì)量標(biāo)準(zhǔn)、檢驗(yàn)方法、操作規(guī)程等的情況均應(yīng)當(dāng)有記錄,并立即報(bào)告主管人員及質(zhì)量管理部門。重大偏差應(yīng)由質(zhì)量管理部門會(huì)同其他部門進(jìn)行徹底調(diào)查,并做好調(diào)查報(bào)告。偏差調(diào)查報(bào)告應(yīng)當(dāng)由質(zhì)量管理部門的指定人員審核并簽字。此外,企業(yè)還應(yīng)當(dāng)采取預(yù)防措施有效防止類似偏差的再次發(fā)生。質(zhì)量管理部門負(fù)責(zé)偏差的分類,保存偏差調(diào)查、處理的文件和記錄。
當(dāng)今社會(huì)科技日趨發(fā)達(dá),社會(huì)系統(tǒng)日漸復(fù)雜,藥品及其包裝的質(zhì)量風(fēng)險(xiǎn)逐漸加大。管理者已經(jīng)不能僅憑經(jīng)驗(yàn)來(lái)掌控產(chǎn)品質(zhì)量,況且很多新出現(xiàn)的現(xiàn)實(shí)問(wèn)題已無(wú)經(jīng)驗(yàn)可以借鑒。而系統(tǒng)論、控制論、信息論可以作為我們更多的理論指導(dǎo),ISO9000族標(biāo)準(zhǔn)、GMP、國(guó)家藥監(jiān)局第13號(hào)令等文件可以給我們提供具體的行動(dòng)指南,藥包材企業(yè)應(yīng)加強(qiáng)對(duì)這些理論和文件的理解和學(xué)習(xí),并以此為基礎(chǔ),做好藥包材質(zhì)量的穩(wěn)定性管理。
2012年11月發(fā)表于《印刷技術(shù)》第22期/總第610期